تاریخچه بیماری ام اس (MS) و شواهد قرون وسطی از مولتیپل اسکلروز
زن جوانی به نام هالدورا (Halldora) که حدود سال 1200 م. در ایسلند زندگی میکرد، ناگهان حرکت و بینایی خود را از دست داد؛ اما پس از دعا به درگاه قدیسان، بعد از هفت روز بهبود یافت. قدیس لیدوینا (Lidwina) اهل اسخیدام (Scheidam) (1380 – 1433 م.)، یک راهبه هلندی، نیز احتمالاً جزو اولین بیمارانی محسوب میشود که واضحاً مبتلا به ام اس بود. از 16 سالگی تا زمان فوتش در 53 سالگی، او از دردهای متناوب، ضعف پاها و از دست دادن بینایی ـ که احتمالا علائم بیماری ام اس بودند ـ رنج میبرد. هر دو بیمار مذکور منجر به پیشنهاد فرضیه “ژن وایکینگ” برای انتشار بیماری شدند.
تقریباً با اطمینان میتوان گفت که آگوستوس فردریک دِاِسته (Augustus Frederick d’Este) (1794-1848)، نوه نامشروع پادشاه بریتانیای کبیر – جرج سوم– مبتلا به بیماری ام اس بود. دِاِسته از خود یک دفترچه خاطرات روزانه باجزئیات برجای گذاشت که شرح 22 سال زندگی او با بیماری بود. دفترچه او اگرچه از سال 1822 شروع شده و در سال 1846 پایان می یابد، اما تا سال 1948 ناشناخته بود. علائم او در 28 سالگی با یک نابینایی گذرا بعد از مراسم تشییع دوستش، آغاز شد. در حین بیماری اش به ضعف پاها، دست و پا چلفتی بودن، بی حسی، گیجی سر (Dizziness)، اختلالات مثانه و اختلال در نعوظ دچار گشت. در سال 1844، شروع به استفاده از صندلی چرخ دار کرد. علی رغم بیماری اش، به زندگی خود خوشبین بود.
گزارش دیگری از بیماری ام اس توسط خاطره نویس انگلیسی ـ بروس فردریک کامینگز (Bruce Frederick Cummings) (1889-1919) با نام مستعار دبلیو.ان.پی باربلیون (W.N.P Barbellion) ـ ثبت شده که در آن، او جزئیات دقیقی از تشخیص و مبارزه خود با بیماری ام اس را یادداشت کرده است. خاطرات او در سال 1919 با عنوان “مجله یک مرد ناامید (The Journal of a Disappointed Man)” چاپ شد.
کشف زودهنگام بیماری ام اس
رابرت کارزول (Robert Carswell) (1793-1857)، پروفسور آسیب شناس آنگلیسی، و جان کرووایلهیر (Jean cruveilhier) (1791- 1873)، پروفسور آناتومی آسیب شناسی فرانسوی، بسیاری از جزئیات بالینی این بیماری را شرح و توصیف نمودند ولی آن را به عنوان یک بیماری متمایز شناسایی نکردند.
جان ـ مارتین شارکو (Jean-Martin charcot) (1825-1893)، یک عصب شناس فرانسوی برجسته در قرن 19 بود که در بیمارستان سالپتغیه (Salpêtrière hospital) در پاریس فعالیت داشت. شارکو بدون شک یکی از شخصیت های مهم در تاریخچه بیماری ام اس است چرا که یافته های او پیشرفت بزرگی برای فهم بالینی بیماری دربرداشت. شارکو اولین کسی بود که در سال 1868، MS را به عنوان یک بیماری متمایز شناسایی کرد. در 1868، شارکو به دقت زن جوانی را معاینه کرد که به یک نوع لرزش (Tremor) ـ از نوعی که قبلاً ندیده بود ـ مبتلا بود. او سایر اختلالات عصبی بیمارش را ـ نظیر گفتار نامنظم و حرکات غیرعادی چشم ـ یادداشت نمود و آن را با سایر بیمارانی که دیده بود، مقایسه کرد. هنگامی که آن زن جوان فوت کرد، او مغزش را تشریح و معاینه کرد و “پلاک ها” یا زخم هایی را ـ که مشخصه MS بودند ـ یافت.
شارکو همچنین معیارهای تشخیصی را، که سه گانه معروف شارکو هستند، برای این بیماری مطرح کرد: دوبینی (دید دوگانه)، آتاکسی (Ataxia) (اختلال در تعادل و هماهنگی) و دیس آرتری (Dysarthria) (دشواری در سخن گفتن یا گفتار نامنظم) که در بیماران خود این علائم را ثبت کرده بود. شارکوت همچنین تغییرات شناختی را مشاهده کرد، به طوری که بیمارانش را با عباراتی نظیر “حافظه ای که به شدت ضعیف است” و “مفاهیمی که به کندی شکل میگیرند” توصیف نمود.
شارکو اولین کسی بود که ارتباطی قطعی بین علائمی که تا اون موقع رمزآلود بودند (امروزه علائم بیماری ام اس دانسته میشوند) و تغییرات آسیب شناسی ای که در نمونه های پس از مرگ مشاهده میشدند، برقرار نمود. برای اولین بار، تقریباً 40 سال پس از کشف ضایعات، این بیماری بالینی توسط شارکو با نام ” sclérose en plaques” توصیف و MS به عنوان یک بیماری کاملاً جداگانه شناخته شد.
شارکو همچنین اولین اطلاعات کامل بافت شناسی از ضایعات ام اس را تهیه کرد که در آن او بسیاری از ویژگی های مهم را ـ نظیر از دست دادن پوشش میلین (Myelin) و تکثیر الیاف و هسته های گلیال (Glial) ـ توصیف نمود.
در نیمه دوم قرن نوزدهم، معاینات علائم ام اس کم کم به چاپ رسیدند: اولین بار توسط دکتر ویلیام موکسون (Dr. William Moxon) در انگلستان در سال 1873 و سپس دکتر ادوارد سگین (Dr. Edward Seguin) در آمریکا در سال 1878. بیشتر معایناتی که پزشکان در آن زمان انجام میدادند، امروزه نیز انجام میشود. چون هر دو پزشک از سیستم ایمنی اطلاعات چندانی نداشتند، نتوانستند آن را به عنوان یک بیماری خودایمنی شناسایی کنند.
همچنین در 1878، بافت شناس و آسیب شناس فرانسوی لوئیس رانویه (Louis Ranvier) میلین را کشف کرد، یک پوشش محافظت کننده به دور اعصاب که در بیماری ام اس تخریب میشود. در بیمارستان سالپتغیه، بیمارستانی در پاریس که او در آنجا فعالیت میکرد، درمان برای بیماران مبتلا به ام اس انجام میشد. رویکرد بیمارستان برای آتاکسی، استفاده از یک دستگاه تعلیق بود که فرد را با تسمه هایی به دور قفسه سینه و زیر بازوها، سرپا نگاه میداشت.
بررسی های بعدی در مورد بیماری ام اس
در اوایل دهه 1900، پژوهشگران مواد شیمیایی ای یافتند که به آنها اجازه میداد سلول های عصبی را با استفاده از میکروسکوپ مشاهده کنند. در سال 1916، دکتر جیمز داوسون (Dr. James Dawson) از اسکاتلند، التهاب و آسیب به میلین را ـ هنگامی که سلول های مغزی مبتلا به ام اس را در میکروسکوپ مشاهده می کرد ـ توصیف نمود. سلول های سازنده میلین یا اولیگودندروسیت ها (Oligodendrocytes) در سال 1928 کشف شدند. سپس در سال 1943، ترکیب میلین کشف شد.
بعد از توصیفات شارکو، یوجین دِویچ (Eugène Devic) (1858-1930)، جوزف بالو (Joseph Balo) (1895-1979)، پاول فردیناند شیلدر (Paul Ferdinand Schidler) (1886-1940) و اوتو ماربورگ (Otto Marburg) (1874-1948) موارد خاصی از بیماری را توصیف کردند.
سر گوردون هولمز (Sir Gordon Holmes) (1876-1965)، عصب شناس انگلیسی در اوایل قرن بیستم، دریافت که لرزش ارادی ناشی از آسیب مخچه ای اشکالاتی در نرخ، گستره، جهت و نیروی حرکت دارد. عصب شناسان تست های بالینی اختصاصی برای ارزیابی لرزش ابداع کردند که شناخته شده ترین آنها تست انگشت به بینی (Finger-to-nose test) و پاشنه پا-ساق پا (Heel-shin test) هستند.
در قرن 20، عصب شناسانی که از توصیفات شارکو استفاده میکردند دریافتند که آتاکسی و لرزش به شدت بیمار را ناتوان میکنند و درمان آنها بسیار دشوار است. لرزش و آتاکسی اساساً ناهماهنگی حرکات عضلات هستند و منجر به حرکات نامتعادل اندام ها و دیگر ماهیچه ها میشوند.
پیشرفت ابزارهای تشخیصی بیماری ام اس
اولین تست تشخیصی قابل اعتماد این بیماری در سال 1913 ـ به واسطه پونکسیون کمری (Lumbar puncture) ـ معرفی شد. در این تست میتوان دریافت که مایع نخاعی حاوی آنتی بادی ها یا پروتئین هایی است که مشخصه بیماری ام اس بوده و با الکتروفورز (Electrophoresis) قابل شناسایی هستند.
پیشرفت های بزرگی نیز در فناوری تصویربرداری تشدید مغناطیسی (Magnetic Resonance Imaging/MRI) در اواخر دهه 1970 به وجود آمد که این فناوری را به عنوان یک ابزار تشخیصی برای ام اس مطرح ساخت. 1981 اولین سالی بود که در آن برای مشاهده مغز بیمار مبتلا به ام اس، از MRI استفاده شد. دکتر آی.آر.یانگ (Dr. I.R. Young) به این افتخار در انگلستان دست یافت و طی چندین سال مشخص شد که این فناوری جدید میتواند آسیب ناشی از MS را ـ حتی در بیمارانی که هیچگونه علائمی از خود بروز نمیدادند ـ به پزشکان نشان دهد.
انجمن های MS
سیلویا لاوری (Sylvia Lawry)، هنگامی که فهمید برادرش به MS مبتلا شده، متوجه شد که هیچ درمان مؤثری برای آن وجود ندارد. پس از انتشار درخواستش در نیویورک تایمز (New York Times)، او بیست عصب شناس را گرد هم آورد و انجمن ملی MS را در آمریکا تأسیس کرد. این باعث تأسیس انجمن های MS در سرتاسر جهان و با یک هدف مشترک شد: که به بیماری ام اس پایان دهند!
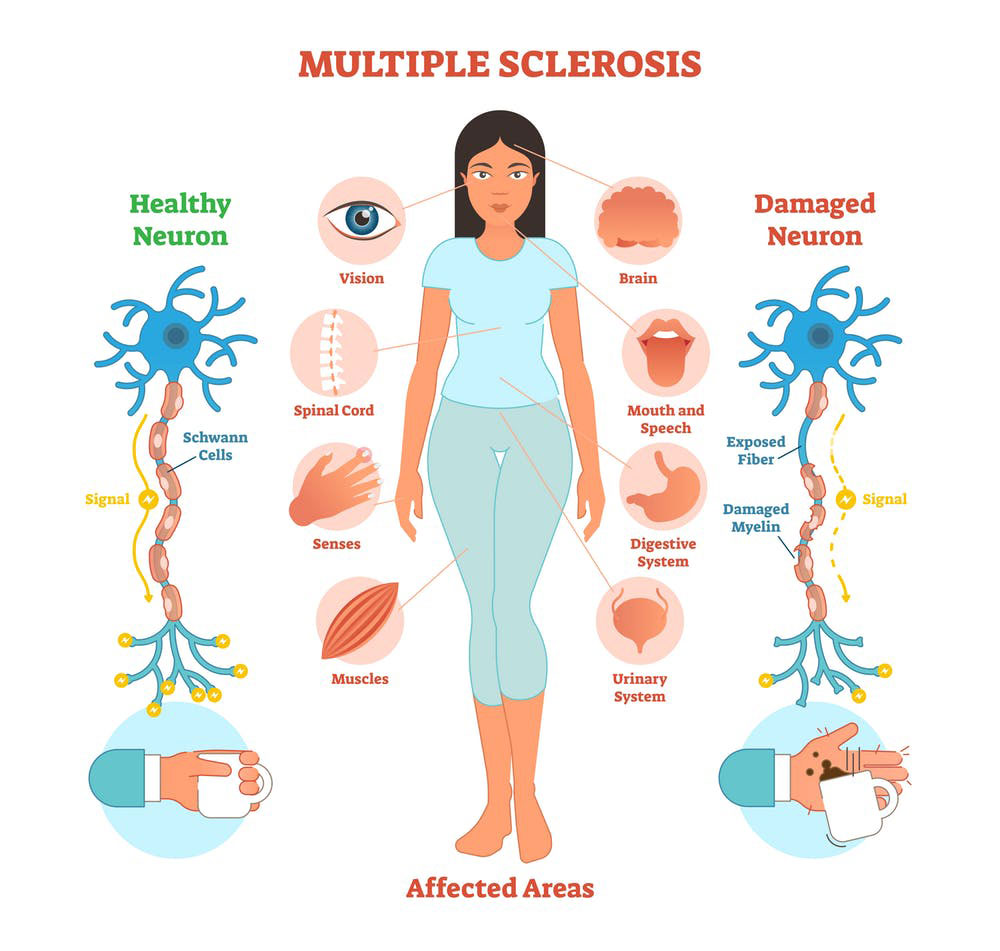
علت بروز بیماری ام اس (MS)
مولتیپل اسکلروز Causes of Multiple Sclerosis (MS)
بیماری ام اس به عنوان یک بیماری سیستم اعصاب مرکزی با ماهیت خودایمنی شناخته می شود که در آن، آسیب غلاف میلین در رشته های عصبی موجود در مغز و نخاع منجر به علایم متنوع عصبی مانند اختلالات حرکتی و حسی می شود. فرضیات مختلفی در سال های اخیر در مورد علت بروز این بیماری مطرح شده که ما در این مطلب به آن ها اشاره خواهیم کرد.
نظریه های اصلی در رابطه با علل ایجاد کننده بیماری ام اس به شرح ذیل است:
عوامل ایمونولوژیک
اکنون به طور کلی پذیرفته شده است که ام اس شامل یک فرآیند خودایمنی – پاسخ غیرطبیعی سیستم ایمنی بدن- علیه میلین در سیستم عصبی مرکزی است. آنتی ژن دقیق یا همان آنتی ژن هدفی که سلولهای ایمنی برای حمله به آن آماده هستند، هنوز ناشناخته مانده است. با این وجود در سالهای اخیر محققان توانسته اند سلولهای ایمنی حمله کننده، برخی از عوامل ایجاد کننده حمله و برخی از مکانها یا گیرنده ها بر روی سلولهای حمله کننده که به نظر میرسد جذب میلین میشود را شناسایی کنند. تلاش های در حال انجام برای کسب اطلاعات بیشتر در مورد روند خودایمنی بیماری ام اس (چیزی که باعث شروع آن میشود، چگونه کار می کند و چگونه کند یا متوقف میشود) محققان را به درک علت بیماری MS نزدیک می کند.
عوامل محیطی
بیماری ام اس در مناطقی که از استوا فاصله بیشتری دارند، بیشتر اتفاق می افتد. متخصصان اپیدمیولوژی (دانشمندانی که الگوهای بیماری را مطالعه می کنند) در تلاشند تا دلیل این عوامل – از جمله تغییرات جغرافیایی، جمعیت شناسی (سن، جنسیت و زمینه قومی)، ژنتیک، علل عفونی و الگوهای مهاجرت – را بررسی کنند. مطالعات بر روی الگوهای مهاجرت نشان داده است که افرادی که در منطقه ای از دنیا با خطر بالای MS متولد میشوند و سپس قبل از 15 سالگی به منطقه ای با خطر کمتر منتقل می شوند، از نظر خطر ابتلا به بیماری مشابه منطقه جدید خود میباشند. چنین داده هایی نشان میدهد که قرار گرفتن در معرض برخی از عوامل محیطی که قبل از بلوغ اتفاق می افتد، ممکن است بعداً فرد را مستعد ابتلا به بیماری MS کند.
برخی دانشمندان فکر میکنند دلیل این امر ممکن است مربوط به ویتامین D – که بدن انسان هنگام قرار گرفتن در معرض نور خورشید به طور طبیعی تولید می کند – باشد. افرادی که در نزدیکی خط استوا زندگی می کنند در طول سال در معرض مقدار بیشتری از نور خورشید قرار میگیرند و در نتیجه آنها مقادیر بالاتری از ویتامین D تولید شده به صورت طبیعی دارند، که تصور می شود تأثیر مفیدی بر عملکرد سیستم ایمنی بدن دارد و ممکن است به محافظت در برابر بیماری های خود ایمنی مانند ام اس کمک کند.
سایر دانشمندان خوشه های ام اس – وقتی تعداد بیمارانی که در یک دوره زمانی خاص و/یا در یک منطقه خاص زندگی میکنند، بیشتر از حد انتظار است – را مطالعه میکنند. این خوشه ها امروزه مورد علاقه دانشمندان هستند چون میتواند سرنخی از عوامل محیطی ای (مانند سموم محیطی و صنعتی، رژیم غذایی یا قرار گرفتن در معرض فلزات کمیاب) داشته باشند که ممکن است باعث ایجاد یا تحریک بیماری گردند. تاکنون مطالعات خوشه ای شواهد روشنی برای وجود هیچ عامل یا عوامل تحریک کننده در بیماری MS به دست نیاورده است.
علل عفونی
از آنجا که قرارگیری اولیه در معرض ویروسها، باکتریها و سایر میکروبها در دوران کودکی اتفاق می افتد، و از آنجا که ویروسها به خوبی به عنوان دلایل از بین رفتن میلین و التهاب شناخته می شوند، ممکن است یک نوع ویروس یا عامل عفونی تحریک کننده ام اس باشد. بیش از ده نوع ویروس و باکتری، از جمله سرخک، دیستمپر سگ سانان (Canine distemper)، ویروس هرپس انسانی -6 (Herpes Simplex Virus-6/HSV-6)، ویروس اپشتین بار (Epstein-Barr virus/EBV) و پنومونی کلامیدیایی مورد بررسی قرار گرفته یا در حال بررسی هستند تا مشخص شود که آیا آنها در ایجاد بیماری ام اس نقش دارند یا نه؛ اما تا به الان به طور قطعی ثابت نشده که این عوامل موجب بیماری MS میشوند.
ژنتیک
در حالی که بیماری ام اس به معنای دقیق بیماری ارثی نیست، داشتن یک خویشاوند درجه یک مانند پدر و مادر یا خواهر و برادر مبتلا به ام اس خطر ابتلا به بیماری در فرد را چندین برابر بیشتر از جمعیت عمومی میکند. مطالعات نشان داده است که شیوع برخی از ژنهای خاص در جمعیتی با میزان بالاتر MS بیشتر است. فاکتورهای ژنتیکی مشترک نیز در برخی از خانواده ها که بیش از یک فرد مبتلا به MS دارند، یافت شده است. برخی از محققان این نظریه را مطرح می كنند كه بیماری ام اس به این دلیل ایجاد می شود كه فردی با نوعی استعداد ژنتیكی متولد میشود که به موجب آن به برخی از عوامل محیطی واكنش نشان می دهد و این واکنش پاسخ خودایمنی ایجاد میکند. تکنیک های پیچیده جدید برای شناسایی ژن ها ممکن است در پاسخ به سؤالات مربوط به نقش ژن ها در پیشرفت MS کمک کند.
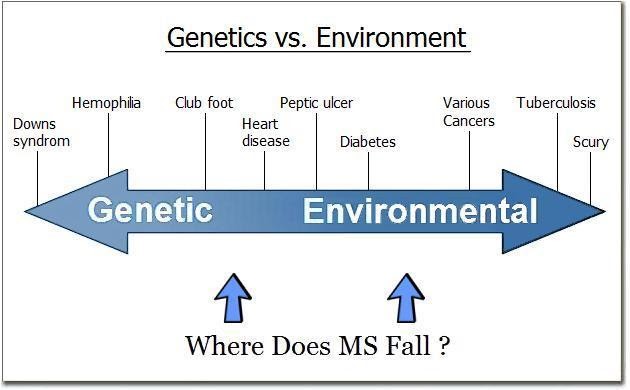
مانند بسیاری از چیزها در زندگی، آیا این محیط یا ژنتیک شما بود که تعیین کرد شما به چه کسی – مبتلا به MS یا غیر مبتلا به آن – تبدیل شده اید؟ ممکن است برخی بگویند یا محیط نقش داشته یا ژنتیک، اما به احتمال زیاد ترکیبی از هر دو و احتمالاً بسیاری از عوامل دیگر وجود دارد. بنابراین بیایید شروع کنیم و سعی کنیم بینشی در مورد چگونگی ابتلا به این بیماری و آغاز مسیر تخریب کننده آن کسب کنیم.
سؤالی که ذهن ما را در هر بیماری درگیر میکند: چرا یک نفر به آن مبتلا میشود و دیگری نه؟ بیایید از یک بیماری مانند سرطان شروع کنیم؛ چگونه سرطان بعضی مواقع انتخاب دقیق و بعضی مواقع انتخاب تصادفی از افراد دارد؟ ممکن است یک فرد سیگاری هرگز به سرطان ریه مبتلا نشود و نیز ممکن است کسی که هرگز سیگار را لمس نکرده و هرگز در معرض دود سیگار نبوده، در 50 سالگی بر اثر سرطان ریه فوت کند – این واقعیت چرا و چطور ممکن است؟ اگر بگوییم دو نفری که ذکر کردیم دوقلو بودند، چه تفاوتی ایجاد میشود؟
همانطور که ژن هایتان به شما در تعیین چگونگی پاسخ شما به برخی از داروها کمک می کنند، کد ژنتیکی شما نیز می تواند روی حساسیت شما به بیماری تأثیر بگذارد. چرا دو نفر با یک سبک زندگی مشابه و یک محیط تقریباً یکسان می توانند چنین تمایلات متفاوتی به بیماری داشته باشند؟ عوامل زیادی از جمله رژیم غذایی در این امر دخیل هستند، اما محققان بر این باورند که یکی از مؤلفه های مهم خطر ابتلا به بیماری، تنوع ژنتیکیِ واکنش افراد در برابر مواد شیمیایی محیطی است.
حال اگر دو نفر دوقلوی همسان داشته باشیم، ساختار ژنتیکی آنها یکسان خواهد بود و آنها تقریباً در معرض یک محیط قرار می گیرند. اگر یکی از این دوقلوها به ام اس و دیگری به پارکینسون مبتلا شود، چه عواملی این مسئله را تعیین میکنند؟
تنوع ژنتیکی میتواند به دلیل تفاوت در مولکول های دئوکسی ریبونکلئیک اسید (Deoxyribonucleic acid/DNA) عامل اثرگذاری باشد. این مولکول ها – که نوکلئوتید نامیده میشوند – شامل آدنین (Adenine)، سیتوزین (Cyrosine)، گوانین (Guanine) و تیمین (Thymine) (A، C، G، T) هستند و در زنجیره های بلندی به نام توالی (Sequence) به هم متصل شده اند. گاهاً اختلافاتی تک حرفی که DNA افراد را متمایز می کند، چندریختی تک نوکلئوتیدی (Single Nucleotide Polymorphism/SNP) نامیده می شود.
بیماری ام اس شایعترین علت عصبی ناتوان کننده در جوانان است و حدود پانصد هزار نفر در ایالات متحده به آن مبتلا هستند. در سراسر جهان، میزان بروز این بیماری تقریباً 1/0 درصد از کل جمعیت است. شمال ایالات متحده و شمال اروپا با بیش از 30 مورد در هر 100000 نفر بیشترین شیوع را دارند.
در صورت داشتن خویشاوندی با بیماری ام اس ، احتمال ابتلا به ام اس افزایش می یابد. اعتقاد بر این است که برخی ترکیب های ژنتیکی احتمال ابتلا به ام اس را در فرد افزایش می دهد. بیشتر افراد فکر میکنند که این افزایش خطر آنقدر زیاد نیست که MS را یک “بیماری ژنتیکی” بنامد. در عوض به نظر میرسد که ژن ها یکی از چندین عواملی هستند که خطر ابتلا به MS را در فرد تعیین می کنند.
میزان MS در بین اعضای خانواده بیشتر است. به طور کلی جمعیت جهان تقریباً 0.25٪ خطر ابتلا به ام اس دارد، در حالی که اعضای خانواده نزدیک فرد مبتلا به MS، مانند کودک یا خواهر و برادر، 3 تا 5٪ احتمال ابتلا به ام اس دارند.
واقعیت این است که دوقلوهای همسان – که دارای ژن های یکسانی هستند – همیشه به MS مبتلا نمیشوند و اکثریت قریب به اتفاق افراد مبتلا به ام اس عضوی دیگری از خانواده که مبتلا به این بیماری باشد، ندارند. بنابراین اگرچه ژن ها ممکن است نقش مهمی داشته باشند، عوامل محیطی دیگری نیز باید وجود داشته باشند.
شانس ابتلا به ام اس در ایالات متحده به شرح زیر است:
| اگر هیچ خویشاوندی مبتلا به ام اس ندارید، 1 در 750 است (جمعیت عمومی). |
| اگر بستگان درجه دوم (پدربزرگ و مادربزرگ، عمه، عمو، خاله، دایی) مبتلا به ام اس دارید، 1 درصد (1 در 100) است. |
| اگر بستگان درجه یک (کودکان، خواهر و برادرها یا دوقلوهای غیرهمسان) مبتلا به ام اس دارید، 2.5 تا 5 درصد است. |
| اگر دوقلوی همسان مبتلا به ام اس دارید، 25 درصد (1 در 4) است. |
در این بخش عوامل مختلفی که ممکن است در MS تأثیر داشته باشند بررسی میشوند. چه محرکی است که روزی بروز می کند و پس از آن حملات شروع می شود؟ این سوالی است که هیچ کس پاسخ آن را نمی داند، زیرا اگر کسی میدانست، بسیار به درمان نزدیک می شدیم یا حداقل برای همیشه از ابتلا به بیماری MS جلوگیری می کردیم.
علت آن هر چه باشد، نتیجه آن ام اس است. همچنین مهم است بدانیم چگونه و چرا ام اس با بسیاری از بیماری های دیگر تفاوت ها و همچنین شباهت هایی دارد.
محیطی
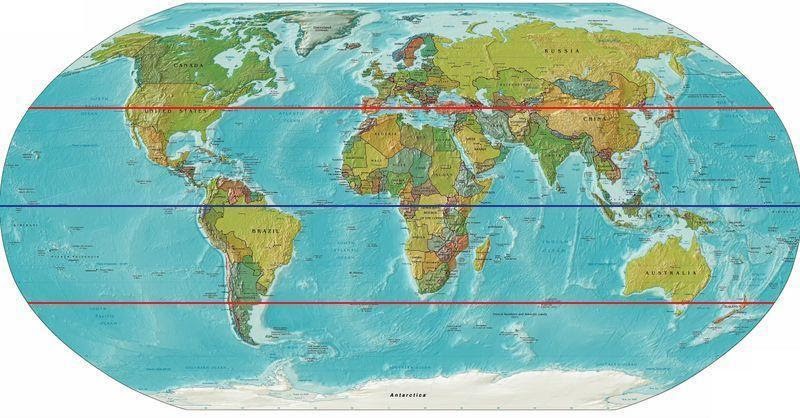
نقشه زیر دارای دو خط قرمز افقی است که در حدود 40 درجه عرض شمالی و جنوبی تنظیم شده اند. نواحی بالاتر از عرض شمالی و پایینتر از عرض جنوبی نقاطی هستند که به طور کلی نرخ بیشتری در بروز MS دارند. توجه داشته باشید که این مناطق اکثر نواحی آمریکای شمالی و اروپا تا روسیه و همچنین انتهای آمریکای جنوبی و استرالیا را شامل میشوند. نواحی بین هر دو خط 40 درجه همچنان دارای موارد جدید بروز ام اس هستند، ولی 5 برابر کمتر.
داده ها نشان داده اند که بیماری MS به ویژه در اسکاتلند، اسکاندیناوی و سرتاسر شمال اروپا شایع است. در ایالات متحده شیوع MS در سفیدپوستان بیشتر از سایر گروه های نژادی است. مطالعات نشان داده اند که این بیماری در مناطق خاصی از جهان شیوع بیشتری دارد، اما اگر قبل از بلوغ از منطقه ای با خطر بالاتر به یکی از مناطق کم خطرتر منتقل شوید، از نظر خطر ابتلا به بیماری ام اس مشابه مکان جدید خود میشوید. این موضوع نشان می دهد که قرار گرفتن در معرض برخی از عوامل محیطی قبل از بلوغ ممکن است فرد را مستعد بیماری MS کند.
ام اس یک بیماری مربوط به آب و هوای معتدل است، یعنی مناطق بین محدوده عرض های جغرافیایی 40 درجه و 60/70 درجه. در هر دو نیمکره، شیوع آن با افزایش فاصله از خط استوا بیشتر میشود.
نظریه های بسیاری وجود دارد که نشان می دهد چرا ام اس در مناطقی که تغییرات دمایی بیشتری دارند در مقایسه با مناطق با دمای ثابت تر، شایع تر است. خطر ابتلا به بیماری با تفاوت های زمانی و جغرافیایی تغییر میکند و ممکن است تحت تأثیر مهاجرت بین مناطق مختلف باشد. تعداد زیادی از علل بالقوه از جمله عفونت، ایمنی زایی، عوامل تنش زای جسمی و عاطفی، آب و هوا، رژیم غذایی و مواجهه شغلی با استفاده از طرح های مختلف مطالعه مشاهده ای مورد مطالعه قرار گرفته اند.
ممکن است به دلیل تغییر در عادات جمعیتی، دمای سردتر باعث گسترش سریعتر ویروس ها شود. حال اگر نوعی ویروس یکی از عوامل اصلی MS باشد، و هوای سردتر هم باعث جمع شدن جمعیت شود، احتمال انتقال ویروس در آنها بسیار زیاد است؛ مانند نحوه انتقال ویروس آنفلوانزا در ماه های زمستان. با وجود تعداد نسبتاً زیاد جمعیت جهان در نزدیکی و بالاتر از عرض جغرافیایی 40 درجه شمالی، گروه های جمعیتی در تمام طول سال به یکدیگر نزدیک هستند. این مناطق که به شدت با صنعتی شدن زودهنگام جهان – از جمله تصفیه بالای فلزات، نفت و آلودگی های بعدی و مختلف – درگیر هستند، بیشترین موارد ابتلا را هم همچنان دربردارند.
همچنین توزیع جغرافیایی بیماری MS و تغییر خطر ابتلا به بیماری در بین مهاجران، شواهدی را در مورد وجود عوامل قدرتمند محیطی در بیماری MS نشان داده است. همچنین میتواند به این معنی باشد که تفاوت مناطق مختلف در رژیم غذایی و سایر رفتارها نیز میتوانند جزو عوامل محیطی باشند.
همچنین چون نواحی نزدیک به خط استوا دائماً گرمتر هستند، ممکن است گروه های جمعیتی، کمی از یکدیگر فاصله داشته باشند. این موضوع احتمالاً می تواند شیوع این نوع ویروس ها را کاهش یابد. همچنین ممکن است که صنعتی شدن اخیر این مناطق باعث شده باشد که عوامل محیطی موجود در این جمعیت ها مدت زمان مورد نیاز خود را برای ایجاد بیماری MS، سپری نکرده باشند.
آیا ممکن است تمایل جهان برای توسعه، نتیجه دیگری برای نیاز مداوم ما به توسعه بیشتر به ارمغان داشته باشد؟ آیا ممکن است ما مسئول این بیماری و احتمالاً بسیاری از بیماری های دیگر باشیم؟ آیا بیماری MS می تواند پیامدی از گرم شدن کره زمین باشد؟
برخی دانشمندان فکر می کنند دلیل این امر ممکن است مربوط به ویتامین D باشد، که بدن انسان هنگام قرار گرفتن در معرض نور خورشید به طور طبیعی تولید می کند. افرادی که در نزدیکی خط استوا زندگی می کنند در طول سال در معرض میزان بیشتری از نور خورشید هستند. در نتیجه آنها مقادیر بالاتری از ویتامین D تولید شده طبیعی دارند، که تصور میشود تأثیر مفیدی بر عملکرد سیستم ایمنی بدن دارد و ممکن است به محافظت در برابر بیماری های خود ایمنی مانند ام اس کمک کند.
برخی از جمعیت ها مانند اسکیموها هرگز به ام اس مبتلا نم یشوند. سرخپوستان بومی آمریکای شمالی و جنوبی، ژاپنی ها و سایر مردم آسیا نرخ بروز بسیار کمی از بیماری MS دارند. به نظر میرسد این موضوع نشان میدهد که ممکن است نوعی سد ژنتیکی در این گروه از افراد وجود داشته باشد که از پیشرفت MS جلوگیری می کند.
همچنین “همه گیری” MS در طول تاریخ وجود داشته است؛ زمانی مردمانی که پس از جنگ جهانی دوم در ساحل دانمارک زندگی می کردند، به آن مبتلا شدند. این موضوع دلیل محیطی ام اس را نشان می دهد.
نشان داده شده کسی که سیگار میکشد 40 تا 80٪ در مقایسه با کسی که نمیکشد خطر ابتلا به ام اس بیشتری دارد. مطالعه ای با بیش از 2000 بیمار مبتلا به بیماری MS و سالم که در Oxford’s Journal of Brain منتشر شد، نشان داد که سیگار کشیدن نه تنها ممکن است خطر ابتلا به ام اس را افزایش دهد، بلکه سیگار کشیدن در کسانی که قبلاً ام اس داشته اند ممکن است باعث شود پیشرفت بیماری تسریع شده و علائم بدتر گردد.
ژنتیک پایه
DNA
ژنتیک انسانی بسیار پیچیده است و حتی در صورت در اختیار داشتن تمام اطلاعات موجود در این ناحیه به سختی میتوان آن را شناخت و تمام موجودیت آن را توصیف کرد. همه چیز در سطح سلولی آغاز میشود؛ با سلول هایی که به عنوان واحدهای اصلی فعالیت هر موجود زنده تلقی میشوند. تمام دستورالعمل های لازم برای هدایت فعالیت های آنها در یک ماده شیمیایی موسوم به DNA وجود دارد.
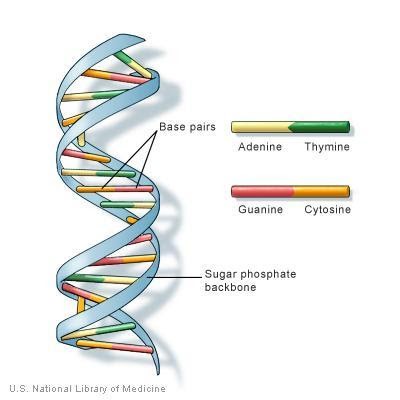
DNA تمام موجودات زنده از اجزای شیمیایی و فیزیکی یکسانی تشکیل شده است. توالی DNA ترتیب خاصی از کنار هم قرار گرفتن بازها در امتداد رشته DNA است. ترتیب خاص ترکیبات شیمیایی آن به دستورالعملهای دقیق مورد نیاز برای ایجاد ارگانیسمی خاص با صفات منحصر به فرد خود تبدیل میشود.
DNA ماده ارثی در انسان و تقریباً همه موجودات دیگر است. بیشتر DNA در هسته سلول قرار دارد؛ جایی که DNA هسته ای نامیده می شود. اما مقدار کمی از آن را میتوان در میتوکندری یافت که DNA میتوکندریایی یا mtDNA نامیده می شود.
اطلاعات موجود در DNA به عنوان کد ذخیره می شود و از چهار باز شیمیایی تشکیل شده است: آدنین (A)، گوانین (G)، سیتوزین (C) و تیمین (T). DNA انسان از حدود 3 میلیارد باز تشکیل شده است و بیش از 99٪ این بازها در همه افراد یکسان است. ژنوم شامپانزه و انسان بیش از 98٪ یکسان است که نشان می دهد اختلاف 1٪ چقدر میتواند قابل توجه باشد. ترتیب یا توالی قرار گرفتن این بازها اطلاعات در دسترس برای ساخت و نگهداری ارگانیسم را تعیین می کند، شبیه روشی که حروف الفبا به ترتیب خاصی برای تشکیل کلمات و جملات ظاهر می شوند.
بازهای DNA با یکدیگر جفت میشوند – A با T و C با G – و واحدهایی به نام جفت باز ایجاد می کنند. هر باز نیز به یک مولکول قند و یک مولکول فسفات متصل است. مجموع یک باز، قند و فسفات را نوکلئوتید مینامند. نوکلئوتیدها در دو رشته بلند مرتب شده اند که مارپیچی به نام مارپیچ دوتایی را تشکیل می دهند. ساختار مارپیچ دوتایی تا حدودی شبیه یک نردبان است، جفت بازها پله های نردبان را تشکیل می دهند و مولکول های قند و فسفات قسمت های عمودی و کناری نردبان را می سازند.
یک ویژگی مهم DNA این است که میتواند از خود نسخه برداری کند. هر رشته DNA در مارپیچ دوتایی میتواند به عنوان الگویی برای تکثیر توالی بازها عمل کند. از نظر شیمیایی، DNA از دو پلیمر بلند به نام نوکلئوتید تشکیل شده است که بخش اصلی آنها از قندها و گروه های فسفات ساخته شده و با پیوندهای استری به یکدیگر متصل شده اند. این دو رشته در جهت مخالف یکدیگر قرار دارند و بنابراین غیرموازی (Anti-parallel) هستند.
هر یک از چهار نوع مولکولی که باز نامیده می شوند، به قند متصل است. توالی این چهار باز در امتداد رشته DNA است که اطلاعات را کد میکند. این اطلاعات با استفاده از کد ژنتیکی – که توالی اسیدهای آمینه درون پروتئین ها را مشخص می کند – رمزگشایی میشود. این کد با کپی کردن بخشهایی از DNA در RNA مرتبط با آن، در فرآیندی به نام رونویسی (Transcription)، رونوشت میشود. این امر هنگام تقسیم سلول ها بسیار حیاتی است زیرا هر سلول جدید باید یک نسخه دقیق از DNA موجود در سلول قدیمی داشته باشد.
ژنوم هر ارگانیسم زنده، مجموعه کامل DNA آنهاست. اندازه ژنومها بسیار متفاوت است و کوچکترین ژنوم شناخته شده برای موجود زنده آزاد (یک باکتری) حاوی حدود 600,000 جفت باز DNA است، در حالی که ژنومهای انسانی حدود 3 میلیارد جفت باز دارند. اکنون به جز سلول های قرمز خون فرد بالغ، تمام سلول های انسانی حاوی یک ژنوم کامل هستند.
کروموزوم ها
در هسته هر سلول، یک مولکول DNA در ساختارهای رشته مانند به نام کروموزوم بسته بندی میشود. هر کروموزوم از یک مولکول DNA که بارها و بارها در اطراف پروتئین هایی به نام هیستون – که ساختار آن را پشتیبانی می کنند – پیچیده شده، تشکیل شده است.
DNA در هر سلول انسانی در 46 کروموزوم بسته بندی شده که 23 جفت هستند. هر کروموزوم از نظر فیزیکی مولکولی از DNA است که طول آن از حدود 50 میلیون تا 250 میلیون جفت باز متغیر میباشد. انواعی از ناهنجاری های بزرگ کروموزومی – از جمله نسخه های از دست رفته یا اضافی، شکستگی های بزرگ و اتصال های مجدد (جا به جایی ها) – با بررسی میکروسکوپی قابل تشخیص است. با این حال بیشتر تغییرات در DNA ظریف تر میباشد و برای یافتن تفاوت هایی مثلاً اختلاف در یک باز، به تجزیه و تحلیل دقیق تری از مولکول DNA نیاز است.
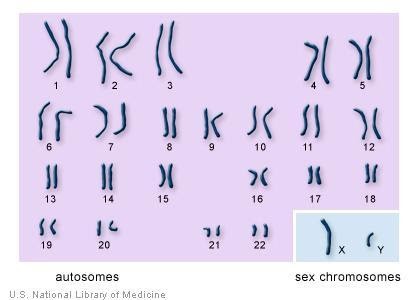
22 جفت از 23 جفت کروموزوم – که کروموزوم های اتوزوم (Autosomes) نامیده می شوند – هم در مردان و هم در زنان یکسان هستند. جفت 23م – کروموزوم های جنسی – بین زن و مرد متفاوت است. زن ها دو نسخه از کروموزوم X دارند در حالی که مردان دارای یک کروموزوم X و یک کروموزوم Y هستند.
22 جفت کروموزوم اتوزوم با اندازه های خود شماره گذاری می شوند. دو کروموزوم دیگر، X و Y، کروموزوم های جنسی هستند. به تصویر بالا که کروموزوم های انسانی که به صورت دوتایی کنار هم قرار گرفته اند، کاریوتایپ (Karyotype) گفته می شود.
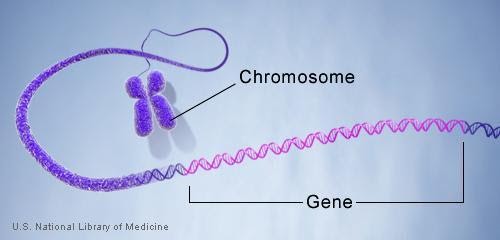
تخمین زده می شود که ژنوم انسان حدود 25000 ژن داشته باشد. اندازه ژن ها از چند صد باز تا حدود 3 میلیون باز متفاوت است.
هر شخص دارای دو نسخه از هر ژن است که هر نسخه از یکی از والدین به ارث رسیده است. بیشتر ژن ها در همه افراد یکسان است، اما کمتر از 1٪ ژن ها کمی متفاوت تر از بقیه هستند. آلل ها اشکالی از یک ژن هستند که تفاوت کمی در توالی بازهای DNA دارند. همانطور که قبلاً بحث شد، این تفاوتهای کوچک ویژگیهای منحصر به فردی به شخص می بخشد.
روند وراثت ژن ها از هر یک از والدین فرآیند بسیار دقیقی است. در موارد نادر ممکن است خطاهایی به دلیل عوامل بیرونی مانند مواد شیمیایی و ویروس ها رخ دهند. بدن فرد معمولاً روش هایی برای اصلاح این خطاها دارد، اما گاهی اوقات این اشتباهات می تواند منجر به تغییر یا جهش های دائمی در توالی ژن ها شود و منجر به بیماری های ارثی گردد.
برخی از بیماری ها مانند فیبروز کیستیک (Cystic fibrosis)، نتیجه به ارث بردن فقط یک ژن جهش یافته است. در بیماری MS و بیماری های خودایمنی، اوضاع پیچیده تر است. اعتقاد بر این است که ژن های متعددی که به طور هماهنگ عمل می کنند در این بیماری ها دخیل هستند، تقریباً به گونه ای که پروتئین های تنظیم کننده سیستم ایمنی تغییر می یابند. جداسازی و شناسایی این ژن ها هدف تحقیقات کنونی در سراسر جهان است.
پروتئین ها
پروتئین ها بیشتر عملکردهای زندگی را انجام داده و حتی اکثر ساختارهای سلولی را تشکیل می دهند. پروتئین ها مولکول های بزرگ و پیچیده ای هستند که از زنجیره ای از ترکیبات شیمیایی کوچک به نام اسیدهای آمینه ساخته شده اند. خواص شیمیایی که 20 اسید آمینه مختلف را از هم متمایز می کند، باعث می شود تا زنجیره های پروتئینی به صورت ساختارهای سه بعدی خاصی پیچ و تاب بخورند که عملکردهای خاص آنها را در سلول تعریف می کند.
مجموعه تمام پروتئین های سلول را پروتئوم (Proteome) آن می نامند. بر خلاف ژنوم، پروتئوم در پاسخ به دهها هزار سیگنال محیطی درون و خارج سلولی میتواند از دقیقه به دقیقه تغییر کند. ساختار شیمیایی و رفتار پروتئین با توالی ژن و تعداد و ماهیت پروتئین های دیگر ساخته شده در همان سلول تعیین میشود. به نظر میرسد مطالعات برای کشف ساختار و فعالیتهای پروتئینی – معروف به پروتئومیکس (Proteomics) – در آینده در صدر تحقیقات سلامتی و بیماری باشد.
ژنتیک
اگرچه MS به معنای کلاسیک یک اختلال ارثی در نظر گرفته نمیشود، اما شواهد موثقی برای حمایت از نقش عوامل ژنتیکی در MS وجود دارد. با این حال مطالعات جمعیت و خانواده نشان داده اند که در سبب شناسی MS، عوامل خطر ژنتیکی نقش اصلی در بیماری زایی ام اس دارند. این مؤلفه ژنتیکی در درجه اول با افزایش خطر نسبی خواهر و برادر افراد مبتلا در مقایسه با جمعیت عمومی نشان داده میشود. تجمع خانوادگی این بیماری از قبل از آغاز قرن 20 مشاهده شده و افزایش خطر برای بستگان درجه یک، درجه دوم و سوم افراد مبتلا به ام اس به خوبی اثبات شده است. تجمع MS در افراد یک خانواده، تأثیر ژنتیک بر استعداد ابتلا به MS را نشان میدهد. مطالعات دوقلوها و فرزندخوانده ها نیز از وجود یک مؤلفه ژنتیکی قوی برای MS پشتیبانی میکنند.
از آنجا که MS در اکثر خانواده ها از الگوهای ساده ارثی پیروی نمیکند، احتمالاً استعداد ابتلا به ام اس تا حد زیادی توسط ژن های متعددی که بالقوه برهم کنش دارند تعیین می شود و هر کدام سهم نسبتاً کمی در خطر کلی ابتلا به بیماری دارند. اعتقاد بر این است که عوامل محیطی مانند سیگار کشیدن و قرار گرفتن در معرض عفونت های ویروسی نیز در این امر دخیل هستند. MS نمونه ای از اختلال با توارث پیچیده است.
بسیاری از بیماری های شایع در انسان به دلیل تغییر ژنتیکی در یک ژن منفرد ایجاد نمیشوند بلکه تحت تأثیر فعل و انفعالات پیچیده بین چندین ژن و همچنین عوامل محیطی و سبک زندگی قرار دارند. اگرچه هم عوامل محیطی و هم سبک زندگی احتمال ابتلا به یک بیماری را در هاله ای از ابهام قرار میدهند، در حال حاضر اندازه گیری و ارزیابی تأثیر کلی آنها بر روند بیماری دشوار است. بنابراین استعداد ژنتیکی یک فرد یا احتمال ابتلای او به بیماری بر اساس ژن ها و عوامل وراثتی بررسی میشود.
تنوع ژنتیکی به دلیل تفاوت های جزئی در توالی DNA، تا حدودی با سلامت و خطر ابتلا به بیماری مرتبط است. از آنجا که والدین ژن خود را به فرزندانشان منتقل می کنند، برخی بیماری ها همانند سایر صفات ارثی – به عنوان مثال برخی از جنبه های ظاهری – در خانواده ها تجمع می یابند. به علاوه برخی از علامت های اپی ژنتیکی (Epigenetic) با برخی از انواع بیماری ها مانند سرطان همراه است. با این وجود باید بدانیم که عوامل زیادی غیر از ژن ها – از جمله رژیم غذایی، ورزش و قرار گرفتن در معرض عوامل محیطی – نیز در سلامتی و بیماری نقش دارند.
نقشه برداری ژنتیکی
اگر استعداد ژنتیکی یک عامل باشد، در نتیجه اثرات محیطی در گذشته ممکن است باعث شود جمعیت فعلی تنها منتظر یک محرک برای شروع MS باشد. یک عامل محرک – چه سایر شرایط محیطی باشد و چه عامل ویروسی – در صورت وجود شرایط مناسب ام اس را به وجود می آورد.
نقشه برداری از ژنوم ایجاد نوعی نقشه ژنتیکی است که قطعات DNA را به کروموزوم ها اختصاص می دهد. بنابراین هنگامی که یک ژنوم برای اولین بار بررسی میشود، نقشه ای وجود ندارد و در طی مراحل نقشه برداری ایجاد میشود. این نقشه با پیشرفت زمان و فن آوری بهبود می یابد و وقتی توالی DNA ژنومی گونه ها کامل شود، به حد اعلای خود رسیده است.
DNA نوعی نوکلئیک اسید است که شامل دستورالعمل های ژنتیکی مورد استفاده در توسعه و عملکرد همه موجودات زنده شناخته شده و برخی ویروس ها می باشد. نقش اصلی مولکول های DNA ذخیره طولانی مدت اطلاعات است. DNA اساساً مجموعه ای از نقشه های اصلی یا نوعی دستورالعمل است، زیرا حاوی اقدامات لازم برای ساخت سایر اجزای سلول ها، مانند پروتئین ها و مولکول های RNA، میباشد. بخشهایی از DNA که حامل این اطلاعات ژنتیکی هستند، ژن نامیده می شوند. سایر توالیهای DNA یا اهداف ساختاری داشته یا در تنظیم میزان استفاده از این اطلاعات ژنتیکی نقش دارند.
DNA درون سلول ها به صورت کروموزوم سازمان یافته است و قبل از تقسیم سلول ها در طی همانند سازی DNA، نسخه برداری می شوند. ارگانیسم های یوکاریوتی (حیوانات، گیاهان، قارچ ها و پروتوزوآها) DNA خود را در داخل هسته سلول ذخیره می کنند، در حالی که DNA پروکاریوت ها (باکتری ها و باکتری های باستانی) در سیتوپلاسم سلول یافت میشود. درون کروموزوم ها، پروتئین های کروماتین مانند هیستون ها DNA را فشرده کرده و سازمان میدهند. این ساختارهای فشرده برهم کنش بین DNA و سایر پروتئین ها را هدایت کرده و به کنترل بخشهایی از DNA که رونویس میشوند، کمک می کند.
این امکان در انسان – با در اختیار داشتن بزرگترین کروموزوم با بیش از 220 میلیون جفت باز طول – وجود دارد که عاملی محیطی یا یک ویروس بتواند به اندازه کافی صدمات ژنتیکی ایجاد کند تا بدن ما را برای مشکلات احتمالی آماده کند. اگر قرار باشد جهش های خاص با گذشت زمان اطلاعات ژنتیکی جمعیتها را به روش خاصی تحت تأثیر قرار دهند، بنابراین در صورت انتقال کد ژنتیکی تغییر یافته به نسل های بعدی، آسیب هم میتواند منتقل شود.
در نظر گرفتن اینکه ساختمان مارپیچ دوگانه DNA سمت چپ فقط 12 جفت باز را نشان میدهد و کروموزوم 1 انسان 220 میلیون جفت باز دارد، باید این احتمال وجود داشته باشد که جهش در یک کروموزوم خاص انسانی بتواند آغازگر بیماری MS باشد. در حال حاضر اعتقاد بر این است که کروموزوم 1 انسان 4220 ژن دارد و این فرصت های بسیاری را برای ایجاد مشکل فراهم می کند.
بسیاری از جهش های شناخته شده باعث سرطان میشوند اما برخی از آنها تغییرات جزئی در سطح ژنتیکی ایجاد کرده طوری که هیچ تغییری در جمعیت مشاهده نمیشود. تغییر در توالی های اسید نوکلئیک توسط جهش ها می تواند باعث اضافه شدن و حذف یک یا چند نوکلئوتید یا جایگزینی جفت بازهای نوکلئوتیدی در توالی DNA شود. یک جهش همچنین می تواند در یک جمعیت به دلیل رانش ژنتیکی (Genetic drift) رخ دهد، که نوعی رویداد تصادفی بوده و ناشی از انتقال محتوای ژنتیکی از یک نسل به نسل دیگر است. علت جهش ممکن است عاملی محیطی یا یک ویروس یا یک رانش ژنتیکی ساده باشد که به طور طبیعی اتفاق می افتد.
ممکن است والد شما در سه نسل پیش ناآگاهانه ازدواج فامیلی انجام داده، یا در یک پالایشگاه مس کار می کرده، یا آب آلوده به فلزات سنگین می نوشیده، یا هر ساله در معرض ویروس های زیادی قرار می گرفته، یا بیش از حد چربی های اشباع و مواد نگهدارنده مصرف میکرده، یا در فصل سرما بخاری نداشته و به همین دلیل فردی در خانواده مبتلا به MS شده باشد. حتی ممکن است توضیح دهد که چرا آنها فرد خوبی بوده و مراقب محیط هستند، با دیگران دوستانه رفتار می کنند و 110 سال هم عمر می کنند. اینها همه حدس و گمان است و هنوز هم شناخته شده نیست و ممکن است هرگز هم شناخته نشود.
با اینکه امروزه میدانیم محیط در وضعیت خوبی قرار ندارد، ویروس ها در اطراف ما وجود دارند و ژنتیک انسان نسبت به جهش ها بسیار آسیب پذیر است، هنوز هم مشخص نیست که علت بیماری MS چه میباشد. این علت ممکن است هرگز هم مشخص نشود، اما آنچه باید روی آن متمرکز شود ادامه جستجو برای یک راه درمان است.
تحقیقات ژنتیکی
گروه ژنتیکی MS (MS Genetic Group/MSGG) شواهدی از ژن استعداد ابتلا به MS در یک منطقه در کروموزوم 6 پیدا کرده است که به عنوان مجموعه سازگاری بافتی اصلی (Major Histocompatability Complex/MHC) شناخته می شود. گروه ژن های MHC به عنوان “کلید اصلی” سیستم ایمنی بدن عمل می کنند. گروه های پژوهشگر دیگری نقش مهم MHC را در کمک به MS تأیید کرده اند و همچنین مناطق کروموزومی دیگری را – که احتمالاً ژن های استعداد ابتلا به MS را در خود دارند -پیشنهاد داده اند.
بیشتر مطالعات ژنتیکی تاکنون در هر زمان فقط یک ژن، نشانگر یا ناحیه را بررسی کرده اند اما با این حال مشخص شده است که MS تحت تأثیر ژن های متعددی قرار دارد. این احتمال وجود دارد که این ژن ها با یکدیگر تعامل داشته باشند، و شاید در همراهی با تأثیرات محیطی، فنوتیپ MS را تولید کنند. این تعاملات پیچیده را می توان با روشهای مختلفی بررسی کرد. همچنین احتمالاً مطالعات آینده MS باید اطلاعات ژنتیکی و زیست محیطی را در جمع آوری و تجزیه و تحلیل داده های خود با هم لحاظ کنند.
پیشرفت در ژنتیک مولکولی و شناسایی خانواده های پرجمعیتی که چندین عضو مبتلا به MS در آنها وجود دارد (خانواده های چندتایی MS/Multiplex MS families)، به تلاش دانشمندان برای کشف ژن های دربردارنده استعداد ابتلا به MS کمک کرده است. از سال 1991، انجمن ملی MS از یک پروژه بین المللی برای جستجوی این ژن ها پشتیبانی کرده است. تیم های تحقیقاتی چالش یافتن تعداد نامشخصی از ژن های دربردارنده استعداد ابتلا به ام اس را به دوش میکشند. این امر مستلزم جستجو در 3 میلیارد باز DNA است که کد ژنهای متعددی را تشکیل میدهند که ژنوم انسان را به وجود می آورند.
دستورالعمل های رمزگذاری شده در ژن ها به زبان بازهای نوکلئوتیدی اصلی DNA متشکل از A ، T ، C و G نوشته شده اند. این بازها مواد شیمیایی حیاتی هستند که DNA از آنها ساخته می شود. نشانگرها مناطقی از DNA در امتداد کروموزوم ها هستند که در رشته حروف ژنتیکی اختلاف داشته به طوری که “پیام” در هر یک از اعضای یک جفت کروموزوم کمی متفاوت است. این تفاوت ها که چندشکلی یا پلی مورفیسم (Polymorphism) نامیده می شوند معمولاً بر سلامت فرد تأثیر نمی گذارد، بلکه به عنوان “پرچم” هایی قابل آزمایش عمل میکنند. دانشمندان می توانند ردیابی کنند که کدام مارکر از مادر یک شخص و کدام یک از پدر آنها گرفته شده است.
نشانگر DNA
بسیاری از خانواده های چندتایی از سراسر جهان توافق کرده اند که در مطالعات پژوهشی شرکت کنند. محققان در این مطالعات به دنبال الگوهایی از محتوایی ژنتیکی هستند که دائماً توسط افراد مبتلا به MS به ارث میرسد. این الگوهای قابل تشخیص نشانگرهای DNA هستند. محققان DNA گلبول های سفید خون افراد خانواده های چندتایی را جستجو میکنند و به دنبال الگوهای قابل تشخیص یا نشانگرهایی در کد DNA هستند که به طور مشترک توسط افراد مبتلا به این بیماری به ارث رسیده است اما در بستگان سالم آنها وجود ندارد.
هنگامی که یکی از این نشانگرها مشخص میشود، محققان بر روی آن ناحیه تمرکز میکنند و به دنبال نشانگرهای دیگری در نزدیکی آن ژن هستند تا بتوان آن را شناسایی کرد. این روند نزدیک شدن به ژن باید برای هر یک از مناطق نشانگر از خانواده های چندتایی تکرار شود تا زمانی که کاملاً شناسایی گردد. تا سال 1996، حدود 20 مکان که ممکن است حاوی ژن های مؤثر در MS باشند شناسایی شده است؛ اما هیچ ژنی که تأثیر زیادی در استعداد ابتلا به ام اس داشته باشد، دیده نشده است.
تجزیه و تحلیل دو تنوع ژنتیکی جدید نشان داد که ارتباط بسیار قابل توجهی با ام اس دارند. این تغییرات در ژن هایی است که عملکرد پروتئینهای پیام رسان یا سایتوکینها را کنترل می کنند. این پروتئین ها سلولهای ایمنی از جمله سلولهای T را تنظیم می کند، سلول هایی که بازیگران اصلی حمله سیستم ایمنی به مغز و نخاع در ام اس هستند. این تغییرات در ژنهای گیرنده اینترلوکین 2 آلفا و گیرنده اینترلوکین 7 آلفا وجود دارد. اینترلوکین 2 و اینترلوکین 7 با سلولهای T تنظیم کننده (T regulatory) مرتبط هستند که قدرت خاموش کردن حمله ایمنی را دارد و شواهدی از اختلال عملکرد این سلولها در MS دیده میشود. اینترلوکین 2 آلفا قبلاً در سایر بیماری های خود ایمنی – من جمله دیابت نوع 1 – نقش داشته است.
همچنین دو مقاله آنلاین چاپ شده در تاریخ 29 ژوئیه 2007 در Nature Genetics در مورد ارتباط گیرنده اینترلوکین 7 آلفا با MS و نحوه تأثیر این پروتئین بر سیستم ایمنی گزارش داده است. یک مقاله توسط دکترها جاناتان هاینز (Jonathan Haines) (مرکز پزشکی دانشگاه وندربیلت (Vanderbilt University Medical Center))، مارگارت پریکاک ونس (Margaret Preicak-Vance) (دانشکده پزشکی دانشگاه میامی میلر (University of Miami Miller School of Medicine)) و یک گروه بین المللی از پژوهشگران که NMSS بخشی از بودجه آن را تأمین کرد، نگاشته شد. این تیم سه ژن احتمالی MS را که با مطالعات قبلی مشخص شده بود کشف کرد اما فقط توانست ارتباط ژن گیرنده اینترلوکین 7 آلفا با MS را تأیید کند. آنها همچنین شواهدی یافتند که نشان می دهد تنوع ژنی می تواند میزان گیرنده اینترلوکین 7 آلفا را – که ممکن است منجر به اختلال در سرکوب مکانیسم خودایمنی شود – تغییر دهد.
اختلالات و بیماری های HLA
ژنتیک به احتمال زیاد در تعیین ابتلا به MS نقش دارد. به طور کلی احتمال ابتلا به MS کمتر از یک دهم درصد است. با این حال اگر یکی از اعضای خانواده به MS مبتلا باشد، بستگان درجه یک آن شخص (والدین، فرزندان و خواهر و برادرها) 1 تا 3٪ خطر ابتلا به آن را دارند. اگرچه ژن خاصی برای ام اس مشخص نشده، اما چندین محقق به این نتیجه رسیده اند که افراد مبتلا به MS بیشتر از افراد فاقد MS، مناطق خاصی را در کروموزوم های خود به ارث می برند. محققان در حال بررسی آنتی ژن لکوسیت انسانی (Human Leukocyte Antigen/HLA) در کروموزوم 6 هستند، زیرا به نظر می رسد الگوهای HLA بیماران MS با کسانی که MS ندارند متفاوت میباشد.
پیشرفت MS احتمالاً تحت تأثیر فعل و انفعالات تعدادی از ژن ها خواهد بود که هریک از آنها به طور جداگانه و به تنهایی، اثر متوسطی دارند. برای تعیین دقیق اینکه کدام ژنها درگیر هستند، تعیین عملکرد آنها و یادگیری اینکه چگونه تعاملات هر ژن با ژنهای دیگر و محیط باعث می شود فرد مستعد ابتلا به ام اس شود، مطالعات بیشتری لازم است. چنین مطالعاتی علاوه بر اینکه به روش های بهتری برای تشخیص ام اس منجر می شود باید سرنخی از علل اصلی بیماری MS و در نهایت درمان های بهتر یا راهی برای جلوگیری از بیماری به همراه داشته باشد.
علائم بیماری ام اس و نشانه های بیماری مولتیپل اسکلروز
علائم بیماری ام اس ممکن است خفیف یا شدید، کوتاه یا طولانی مدت باشند و ممکن است در ترکیب های گوناگونی ظاهر شوند. تظاهرات بیماری با ناحیه درگیر در سیستم عصبی مرکزی (Central Nervous System/CNS)، تعداد و شدت نواحی آسیب دیده تعیین می شود. علائم بیماری در تقریباً 70 درصد از بیماران مبتلا به ام اس، به خصوص کسانی که در مراحل ابتدایی آن قرار دارند، به صورت جزئی یا کامل بهبود خواهند یافت. برای مطالعه توضیحات کامل در مورد علائم بیماری ام اس اینجا کلیک کنید.







