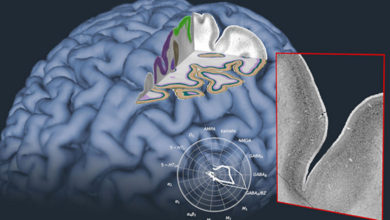
اینترفرون بتا: اولین درمان تأیید شده برای ام اس
اینترفرون های بتا (Beta interferon) اولین دسته دارویی بودند که برای درمان ام اس عودکننده-بهبودیابنده (Relapsing-Remitting MS/RRMS) تأیید شد.
اینترفرون های بتایی که برای اشکال عودکننده ام اس تأیید شده اند، عبارتند از:
- آونکس (Avonex) (اینترفرون بتا-1 آ (Interferon beta-1a))
- ربیف (Rebif) (اینترفرون بتا-1 آ (Interferon beta-1a))
- بتاسرون (Betaseron) (اینترفرون بتا-1ب (Interferon beta-1b))
- اکستاویا (Extavia) (اینترفرون بتا-1ب (Interferon beta-1b))
بتاسرون برای اولین بار در سال 1993 تأیید شد. پگ اینترفرون بتا-1 آ (Peginterferon-beta 1a) (پلگریدی (Plegridy)) که مدت زمان عمل آن طولانی تر است، در سال 2014 تأیید شد.
اینترفرون های مورد نیاز برای ام اس به صورت تزریقی یا از طریق تزریق عضلانی یا از طریق تزریق زیر جلدی (زیر پوست) تجویز می شوند. می توانید به منظور راحتی خود برای انجام این تزریق آموزش ببینید. به علاوه، برخی از فرمولاسیون ها جهت سهولت در تجویز، به صورت سرنگ از پیش پر شده یا قلم انژکتور خودکار (Autoinjector pen) ارائه می شوند.
تزریقات از یک روز در میان تا هر دو هفته یکبار، بسته به نوع دارو و دستور مصرف، انجام می شوند.
عوارض جانبی اینترفرون بتا
تحمل عوارض جانبی اینترفرون ها (به عنوان مثال به آونکس مراجعه کنید) برای برخی از بیماران می تواند دشوار باشد و ممکن است پایبندی شما به درمان را کاهش دهد، برای مثال:
- علائم شبه آنفولانزا و واکنش های محل تزریق در اینترفرون ها رایج است.
- واکنش های آلرژیک، افسردگی و مسمومیت کبد عوارض جانبی جدی تر اما کمتر شایع اینترفرون بتا هستند. برای کنترل عملکرد کبد باید آزمایشات خونی انجام دهید.
- در خون برخی از بیماران ممکن است آنتی بادی هایی علیه اینترفرون بتا ایجاد شود و این بیماران در برابر درمان مقاوم گردند؛ به عبارتی ممکن است اثر دارو کاهش یابد و بیمار به تغییر درمان خود نیاز پیدا کند.
نه عوارض جانبی بیماران مختلف یکسان است نه میزان بروز آنها. برخی از واکنش ها، مانند علائم شبه آنفولانزا، ممکن است در ابتدای درمان شایع تر باشد.
حتماً عوارض جانبی احتمالی درمان و میزان آنها را با پزشک خود در میان بگذارید.
کوپاکسون و گلاتوپا: داروهای احتمالی در خط اول درمان
کوپاکسون (Copaxone) از صنایع دارویی توا (Teva) و گلاتوپا (Glatopa) از شرکت ساندوز (Sandoz) هر دو محتوی گلاتیرامر (Glatiramer) هستند که به عنوان یک عامل کنترل کننده بیماری و تعدیل کننده سیستم ایمنی برای بیماری ام اس عودکننده-بهبودیابنده (RRMS) در نظر گرفته می شود، از جمله سندرم بالینی منفرد (Clinically isolated syndrome/CIS)، بیماری عودکننده-بهبودیابنده و بیماری پیش رونده ثانویه (Secondary progressive disease) فعال).
گلاتیرامر ام اس را درمان نمی کند اما می تواند میزان وقوع عود را کمتر کند.
گلاتوپا یک نسخه قابل تعویض با ژنریک اختصاصی (Branded generic) از کوپاکسون است. یک شکل ژنریک از گلاتیرامر، ساخته شده توسط صنایع دارویی مایلن (Mylan)، نیز در بازار موجود است.
عوارض جانبی شایع گلاتیرامر عبارتند از:
- واکنش های محل تزریق
- گرگرفتگی
- درد قفسه سینه
- واکنش های پس از تزریق (اضطراب، درد قفسه سینه، تپش قلب، تنگی نفس، گرفتگی گلو، گرگرفتگی).
عوارض جانبی تزریق به طور معمول 15 تا 30 دقیقه طول می کشند، بدون درمان برطرف می شوند و عوارض درازمدتی هم برای آنها دیده نشده است.
داروهای خوراکی جدید ام اس
ترکیبات اینترفرون بتا یا گلاتیرامر می توانند اولین گزینه بسیاری از پزشکان برای درمان ام اس باشند. داروهای “ABC” (آونکس (A)، بتاسرون (B) و کوپاکسون (C)) غالباً سه داروی مورد استفاده در خط اول درمان هستند که برای درمان طولانی مدت بیماری ام اس استفاده می شوند.
با این حال عوارض جانبی و سختی ناشی از تزریق در این درمان ها غالباً مشکل ساز است و درمان های خوراکی جدید در حال حاضر انتخاب های بی نظیری را برای بیماران مبتلا به ام اس عودکننده-بهبودیابنده و ام اس پیشرونده ثانویه (SPMS) ارائه می دهد.
- گیلنیا (Gilenya) (فینگولیمود (Fingolimod)) اولین درمان خوراکی برای ام اس است که توسط سازمان غذا و دارو (FDA) در سال 2010 تأیید شد.
- این دارو برای درمان اشکال عودکننده بیماری ام اس در بیمارانی با سن بالای 10 سال توصیه می شود.
- در سال 2018، گیلنیا اولین تأییدیه FDA را به عنوان دارویی برای درمان ام اس در اطفال مبتلا به این بیماری، دریافت کرد.
سایر درمان های خوراکی که از زمان تأیید گیلنیا در دسترس بیماران قرار گرفته اند، عبارتند از:
- اوباجیو (Aubagio) یا تری فلوناماید (Triflunomide) در سال 2012
- تکفیدرا (Tecfidera) یا دی متیل فومارات (Dimethyl fumarate) در سال 2013
- مایزنت (Mayzent) یا سیپونیمود (Siponimod) در سال 2019
- ماونکلاد (Mavenclad) یا کلادریبین (Cladribine) در سال 2019
- ویویومریتی (Vumerity) یا دیروکسیمل فومارات (Diroximel fumarate) در سال 2019
- بافیرتام (Bafiertam) یا مونومتیل فومارات (Monomethyl fumarate) در سال 2020
- زپوسیا (Zeposia) یا اوزانیمود (Ozanimod) در سال 2020
- پونوری (Ponvory) یا پونزیمود (Ponesimod) در سال 2021
گیلنیا (فینگولیمود)
تصور می شود گیلنیا (Gilenya) با جلوگیری از ورود گلبول های سفید خون (لنفوسیت ها) به سیستم عصبی مرکزی (Central nervous system/CNS) و ایجاد التهاب و آسیب به سلول های عصبی، عمل می کند.
در مطالعات بالینی نشان داده شده که گیلنیا در مقایسه با یک سال مصرف اینترفرون بتا -1 آ، یا در مقایسه با دو سال مصرف دارونما، عود بیماری را به کمتر از نصف میزان آن کاهش می دهد. به علاوه در یک سال، تعداد بیمارانی که از عود رهایی یافته بودند در آن هایی که گیلنیا مصرف می کردند نسبت به کسانی که از اینترفرون بتا-1 آ استفاده می کردند 13 درصد بیشتر بود. همچنین نشان داده شده که گیلنیا پیشرفت بیماری را کند و تعداد ضایعات مغزی در MRI را کاهش می دهد. گیلنیا توسط نوارتیس (Novartis) تولید می شود.
عوارض جانبی شایع (> 10 درصد) در صورت مصرف گیلنیا عبارتند از:
- سردرد
- افزایش آنزیم های کبدی
- اسهال
- سرفه کردن
- آنفولانزا
- سینوزیت
- کمردرد
- درد شکم (معده)
- درد در اندام انتهایی
سایر هشدارها و عوارض جانبی مهم از جمله اطلاعات مربوط به مصرف گیلنیا در دوران بارداری (با جزئیات بیشتر) را مطالعه کنید.
این دارو در کشور ما نیز توسط شرکت های دارویی متعدد و با نام های تجاری مختلف عرضه می شود. جهت کسب اطلاعات بیشتر در مورد این دارو اینجا را بخوانید.
اوباجیو (تری فلونوماید)
اوباجیو (Aubagio) (تری فلونوماید) با کاهش التهاب و تعداد گلبول های سفید خون در سیستم عصبی مرکزی و محافظت از اعصاب، به عنوان دارویی برای ام اس مصرف می شود. مکانیسم آن مهار دی هیدرواوروتات دهیدروژناز (Dihydroorotate dehydrogenase) است، آنزیمی که در سنتز پیریمیدین (Pyrimidine) نقش دارد.
در آزمایشات بالینی، با مقایسه دوز خوراکی 14 میلی گرمی اوباجیو با دارونما، کاهش قابل توجهی در سه معیار مشخص کننده فعالیت MS مشاهده شد: عود (کاهش 31 درصدی)، پیشرفت ناتوانی (کاهش 30 درصدی) و ضایعات مغزی در MRI (کاهش 80 درصدی).
عوارض جانبی شایع اوباجیو عبارتند از:
- سردرد
- نازک شدن موها (آلوپسی (Alopecia))
- اسهال
- حالت تهوع
- افزایش در آزمایشات عملکردی کبد
- علائم شبه آنفولانزا
- بی حسی یا گزگز دست یا پا (پارستزی (Paresthesia)).
آسیب کبدی، افزایش خطر ابتلا به عفونت ها و افزایش فشار خون از دیگر عوارض جانبی کمتر شایع اما جدی تر این دارو می باشند. برای کنترل عملکرد کبد و شمارش سلول های خونی به آزمایشات منظم خون نیاز دارید.
استفاده از اوباجیو در دوران بارداری
اثرات اوباجیو می تواند به مدت 2 سال پس از قطع درمان در بدن باقی بماند و حتی ممکن است درمان خاصی برای حذف دارو مورد نیاز باشد. اگر مصرف اوباجیو را قطع کردید، تا زمانی که تأیید شود غلظت تری فلونوماید در پلاسما کمتر از 0.02 میلی گرم در لیتر (0.02 میکروگرم بر میلی لیتر) است باید از روش های پیشگیری از بارداری استفاده کنید.
اوباجیو می تواند منجر به نقایص شدید هنگام تولد شود. برای مصرف این دارو دستورالعمل های خاصی وجود دارد که زنان در سنین باروری و نیز مردان باید از آنها پیروی کنند.
این دارو در کشور ما نیز توسط شرکت های دارویی متعدد و با نام های تجاری مختلف عرضه می شود. جهت کسب اطلاعات بیشتر در مورد این دارو اینجا را بخوانید.
تکفیدرا (دی متیل فومارات)
نحوه عملکرد تکفیدرا (Tecfidera) (دی متیل فومارات) در ام اس کاملاً مشخص نیست، اما یک مسیر شیمیایی را در بدن فعال می کند که به محافظت از سلول های عصبی در برابر آسیب و التهاب کمک می کند.
در آزمایشات بالینی نشان داده شده که تکفیدرا مشابه سایر درمان ها در درمان ام اس مفید واقع شده است: این دارو عود را کاهش می دهد، کمک می کند تا پیشرفت ناتوانی جسمی به تأخیر بیفتد و نیز تعداد ضایعات مغزی را کم می کند. تکفیدرا توسط بیوژن آیدک (Biogen Idec) تولید می شود.
- در یک مطالعه 2 ساله، 27 درصد از کسانی که تکفیدرا مصرف می کردند در مقایسه با 46 درصد از افرادی که قرص دارونما مصرف می کردند (فاقد دارو)، دچار عود شدند.
- به علاوه، در کسانی که تکفیدرا مصرف می کردند، نسبت به افرادی که دارونما مصرف می کردند، 38 درصد کمتر دچار پیشرفت معلولیت شدند و سرعت توسعه ضایعات مغزی در MRI تا 90 درصد کاهش یافته بود.
عوارض جانبی شایع (> 10 درصد) عبارتند از: گرگرفتگی (قرمزی، خارش و راش)، درد معده، اسهال و حالت تهوع. این عوارض جانبی در ابتدای درمان ظاهر می شوند و ممکن است با گذشت زمان از بین بروند. مصرف تکفیدرا همراه با غذا می تواند به کاهش گرگرفتگی کمک کند.
یک آزمایش خون ساده، قبل از شروع درمان و سپس در ادامه به طور منظم، برای نظارت بر تعداد گلبول های سفید خون شما انجام می شود. در صورت ایجاد عفونت جدی، پزشک ممکن است تا زمان رفع این مشکل از درمان خودداری کند.
در آوریل 2020، بافیرتام (مونومتیل فومارات) توسط FDA تایید شد. بافیرتام یک جایگزین هم ارز زیستی (Bioequivalent) برای تکفیدرا (دی متیل فومارات) است.
این دارو در کشور ما نیز توسط شرکت های دارویی متعدد و با نام های تجاری مختلف عرضه می شود. جهت کسب اطلاعات بیشتر در مورد این دارو اینجا را بخوانید.
ویومریتی (دیروکسیمل فومارات)
تکفیدرا ممکن است برای معده برخی از افراد مبتلا به ام اس بسیار نامطلوب باشد. برای این بیماران جایگزینی وجود دارد.
FDA در اکتبر 2019 کپسول های ویومریتی (دیروکسیمل فومارات)، محصول بیوژن/آلکرمس (Biogen/Alkermes)، را برای درمان انواع عودکننده ام اس (از جمله سندرم بالینی منفرد، بیماری عودکننده-بهبودیابنده و بیماری پیش رونده ثانویه فعال) تأیید کرد.
ویومریتی ساختار شیمیایی متمایزی دارد که ممکن است باعث تحریک نسبتاً کمتر معده شود. ویومریتی پس از ورود به بدن، به مونومتیل فومارات تبدیل می شود، همان متابولیت فعال تکفیدرا یا دی متیل فومارات (محصول بیوژن). این ماده نوعی پیش دارو محسوب می شود.
- پیامد اولیه ویومریتی در یک مطالعه رو در رو (Head-to-head study) با تکفیدرا یا دی متیل فومارات، این بود که علائم کلیدی گوارشی در مصرف آن کمتر گزارش شده بود.
- در یک مطالعه پنج هفته ای، نسبت بیمارانی که به دلیل عوارض جانبی گوارشی درمان را متوقف کردند، 0.8 درصد برای ویومریتی و 4.8 درصد برای دی متیل فومارات بود.
به طور کلی، شایع ترین عارضه جانبی گزارش شده در این مطالعه برای هر دو گروه درمانی، گرگرفتگی، اسهال و حالت تهوع (32.8٪، 15.4٪ و 14.6٪ برای ویومریتی؛ 40.6٪، 22.3٪ و 20.7٪ برای تکفیدرا) بود.
تایسبری و لمترادا : برای ام اس در حال پیشرفت
تایسبری (Tysabri) (ناتالیزوماب (Natalizumab)) و لمترادا (Lemtrada) (آلمتوزوماب (Alemtuzumab)) عموماً برای بیمارانی با ام اس عودکننده که نمی توانند سایر داروهای ام اس را تحمل کنند یا پاسخ ضعیفی به آنها دارند، توصیه می شود.
تیسابری هر 4 هفته یکبار از طریق تزریق درون وریدی (Intravenous/IV) تجویز می شود و می تواند با لوکوانسفالوپاتی چندکانونی پیشرونده (Progressive multifocal leukoencephalopathy/PML)، یک بیماری مغزی نادر اما اغلب کشنده، مرتبط باشد.
اگر تایسبری مصرف می کنید و آنتی بادی JCV در شما مثبت باشد یا بشود (خصوصاً اگر شاخص آنتی بادی حین درمان 0.9 یا بالاتر باشد)، پزشک ممکن است با شما درباره تغییر دارو به یک داروی دیگر که خطر PML پایین تری دارد، گفتگو کند. آنتی بادی JCV مثبت به این معنی است که ممکن است شما با درمان های دارویی خاصی خطر ابتلا به PML را در خود افزایش دهید.
داروهای دیگر مورد استفاده در ام اس که حاوی هشدارهایی برای PML هستند، عبارتند از: آلمتوزوماب یا لمترادا، فینگولیمود یا گیلنیا، ریتوکسیماب (Rituximab) یا ریتوکسان (Rituxan)، اوکرلیزوماب (Ocrelizumab) یا اکرووس (Ocrevus)، دی متیل فومارات یا تکفیدرا، دیروکسیمل فومارات یا ویومریتی، کلادریبین یا ماونکلاد و سیپونیمود یا مایزنت.
اکرووس و کسیمپتا
اکرووس (اوکرلیزوماب)، محصول شرکت دارویی ژنتک (Genetech)، در مارس 2017 تأیید شد.
اکرووس یک آنتی بادی مونوکلونال (Monoclonal antibody) است که به طور انتخابی سلول های B با مارکر CD20 (CD20-positive B cells) را مورد هدف قرار می دهد.
- این دارو اولین درمانی است که برای بیماری ام اس پیشرونده اولیه (Primary progressive MS/PPMS) تأیید شده است.
- همچنین برای بیماری عودکننده (RMS)، شامل سندرم بالینی منفرد، بیماری عودکننده-بهبودیابنده و بیماری پیشرونده ثانویه فعال، توصیه می شود.
- اکرووس به صورت تزریق درون وریدی مصرف می شود. قبل از شروع درمان باید کورتیکواستروئید و آنتی هیستامین داده شود. اکرووس دو بار در سال (هر 6 ماه یک بار) بعد از دوز بارگیری اولیه تجویز می شود.
مطالعات فاز سوم نشان داده که اکرووس روند ناتوانی را در هر دو نوع ام اس کند کرده و نشانه های فعالیت بیماری در مغز (ضایعات MRI) را کاهش می دهد. در گروه RMS، عودهای سالانه تقریباً به نصف کاهش می یابد.
عوارض جانبی خفیف تا متوسط این دارو عبارتند از:
- واکنش های تزریق
- عفونت های تنفسی
- عفونت های پوستی
کسیمپتا (Kesimpta) یا اوفاتوموماب (Ofatumumab)، یک آنتی بادی سیتولیتیک علیه CD20 (CD20-directed cytolytic antibody)، نیز در آگوست 2020 تأیید شد. این دارو برای درمان انواع عود کننده ام اس مورد استفاده قرار می گیرد که شامل سندرم بالینی منفرد، بیماری عودکننده-بهبودیابنده و بیماری پیشرونده ثانویه فعال می باشد. کسیمپتا محصول شرکت نوارتیس، اولین درمان مبتنی بر سلول B است که تجویز آن توسط خود بیمار در خانه انجام می شود و ماهی یک بار به صورت زیرجلدی تزریق می گردد.
این دارو در کشور ما نیز عرضه می شود. جهت کسب اطلاعات بیشتر در مورد این دارو اینجا را بخوانید.
تنظیم کننده های گیرنده اسفنگوزین-1-فسفات
ام اس پیشرونده ثانویه (SPMS) مرحله ای از ام اس است که پس از مرحله اول ام اس، یعنی ام اس عودکننده-بهبودیابنده، رخ می دهد. در SPMS ناتوانی به طور پیوسته ای شدیدتر می شود.
از مارس 2019، سه تنظیم کننده گیرنده اسفنگوزین-1-فسفات جدید (S1P و S1P1) (Sphingosine-1-Phosphate Receptor Modulators)
برای درمان انواع عودکننده ام اس، از جمله سندرم بالینی منفرد، بیماری عودکننده-بهبودیابنده و ام اس پیشرونده ثانویه فعال، تأیید شده است. نحوه عملکرد این داروهای جدید دقیقاً مشخص نیست اما تصور می شود که تنظیم کننده های S1P و S1P1 با گیرنده های کلیدی ای در گلبول های سفید خون (لنفوسیت ها) در سیستم ایمنی متصل می شوند. این عمل به جلوگیری از گسترش لنفوسیت ها به مغز و نخاع بیمار، جایی که می توانند باعث آسیب عصبی شوند، کمک می کند.
FDA در مارس 2019، قرص های روزی یکبار مایزنت (سیپونیمود)، محصول نوارتیس، را برای درمان بزرگسالان مبتلا به انواع عودکننده بیماری ام اس تأیید کرد.
- مایزنت با میل بالایی به گیرنده های S1P1 و S1P5 متصل می شود.
- عوارض جانبی شایع مایزنت (در حداقل 10 درصد از بیماران) در مطالعات شامل سردرد، فشار خون بالا و آزمایشات عملکرد کبدی بالا بود.
کپسول های خوراکی زپوسیا (Zeposia) یا اوزانیمود (Ozanimod) با مصرف روزی یکبار، یکی دیگر از تنظیم کننده های گیرنده S1P، محصول شرکت بریستول-مایرز اسکوئیب (Bristol-Mayers Squibb)، در مارس 2020 تأیید شد.
- زپوسیا نیز با میل بالایی به گیرنده های S1P1 و S1P5 متصل می شود.
- عوارض جانبی (در حداقل 4 درصد از بیماران) ممکن است شامل عفونت دستگاه تنفسی فوقانی، افزایش آنزیم های کبدی، فشار خون پایین هنگام ایستادن، عفونت مجاری ادراری، کمردرد و فشار خون بالا باشد.
FDA داروی خوراکی با مصرف روزی یکبار پونوری (Ponvory) یا پونسیمود (Ponesimod)، محصول شرکت جانسن (Janssen)، را در مارس 2021 برای درمان انواع عودکننده بیماری ام اس تأیید کرد.
- پونوری یک تنظیم کننده S1P1 است که با میل بالایی به گیرنده S1P1 متصل می شود.
- عوارض جانبی شایع (در حداقل 10٪ از بیماران) ممکن است شامل عفونت دستگاه تنفسی فوقانی، افزایش آنزیم های کبدی و فشار خون بالا باشد.
ماونکلاد (کلادریبین)
ماونکلاد (Mavenclad) (کلادریبین) توسط FDA در مارس 2019 برای بیماری عودکننده-بهبودیابنده و بیماری پیشرونده ثانویه فعال تایید شد. ماونکلاد به دلیل پروفایل ایمنی آن، برای بیماران مبتلا به سندرم بالینی منفرد و همچنین به عنوان داروی خط اول، توصیه نمی شود.
ماونکلاد که محصول شرکت ای ام دی سرونو (EMD Serono) است، به عنوان یک آنتی متابولیت پورین (Purine antimetabolite) طبقه بندی می شود. تصور می شود ماونکلاد از طریق ایجاد اختلال در سنتز DNA، اثرات سایتوتوکسیک (Cytotoxic) خود را بر لنفوسیت های B و T (گلبول های سفید خون) اعمال می کند و منجر به از بین رفتن آنها می شود. در مطالعات کنترل شده با دارونما، ماونکلاد تعداد عودها و میزان پیشرفت ناتوانی را به صورت قابل توجهی کاهش داد.
عوارض جانبی شایع گزارش شده شامل عفونت های دستگاه تنفسی فوقانی، سردرد و کاهش تعداد گلبول های سفید خون (لنفوسیت) بود. ماونکلاد نباید در بیماران مبتلا به سرطان فعال یا در زنان باردار، به دلیل آسیب به جنین، استفاده شود.
آیا داروهای اصلاح کننده بیماری به علائم MS کمک می کند؟
داروهای اصلاح کننده بیماری ممکن است به شما کمک نکند که به محض شروع حمله ام اس احساس بهتری داشته باشید، بلکه عمل این داروها کمک به کاهش شانس حمله ام اس و کاهش سرعت بدتر شدن بیماری است. خود حملات غالباً نیاز به درمان های متفاوتی دارند.
- به عنوان مثال، کورتیکواستروئیدهایی مانند پردنیزولون خوراکی یا متیل پردنیزولون (دپومدرول) درون وریدی می توانند برای کاهش التهاب در ام اس استفاده شوند.
- تعویض پلاسما یا پلاسما فرز (Plasmapheresis) برای درمان علائم شدید در بیمارانی که به کورتیکواستروئیدها پاسخ نمی دهند، مورد استفاده قرار گرفته است.
- آمپیرا (Ampyra) یا دالفامپریدین (Dalfampiridine)، محصول شرکت صنایع دارویی آکوردا (Acorda therapeutics)، یک مسدود کننده کانال پتاسیم با مصرف خوراکی است. آمپیرا، راه رفتن را در مبتلایان به ام اس بهبود می بخشد. اگر سابقه تشنج یا بیماری کلیوی دارید، نباید از این دارو استفاده کنید. اگر آمپیرا در دوزهای بیشتر از مقدار توصیه شده (10 میلی گرم دو بار در روز) داده شود، می تواند باعث تشنج گردد.
چه باید بکنید: یک سبک زندگی سالم برای بیماران مبتلا به ام اس
با ایجاد رفتارهایی در سبک زندگی خود و اجتناب از یک سری محرک ها، می توان بیماری ام اس را بیشتر کنترل کرد. همه بیماران مبتلا به ام اس باید در حین کار با تیم مراقبت های بهداشتی خود، به سمت دستیابی به این اهداف تلاش کنند:
- انجام فیزیوتراپی.
- خودداری از سرما یا گرمای شدید.
- مصرف رژیم غذایی سالم و متعادل.
- عدم مصرف سیگار و مواجهه با دود سیگار.
- آموزش دیدن در مورد داروهای مختلف خود و پرسیدن سؤال اگر چیزی را متوجه نشدید.
- ورزش به طور منظم.
- کاهش استرس.
- یافتن حمایت عاطفی.
چگونه می توان تشخیص داد که کدام درمان مناسب است؟
ام اس یک بیماری پیچیده است که نیاز به توجه و درمان منحصر به فرد از سوی تیم اختصاصی ارائه دهندگان مراقبت های بهداشتی دارد. تصمیم گیری در مورد درمان دارویی با در نظر گرفتن ویژگی های فردی شما و مشخصات بیماریتان انجام می شود، به عنوان مثال:
- سبک زندگی شما
- شرح حال بیماری ام اس
- ملاحظات کار و زندگی در خانه
- پروفایل عوارض جانبی و هزینه های مربوط به گزینه های درمانی شما.
با گذشت زمان و بهبود وضعیت و درمان شما، این بحث ها را با پزشک خود ادامه دهید. هر فرد به روش های مختلف به درمان ام اس پاسخ می دهد، بنابراین رویکرد شخصی سازی شده بهترین راه برای اخذ نتیجه مثبت است.